美國食品藥品監督管理局(FDA)正重新調整針對新冠加強針的使用政策。根據FDA專員Marty Makary與疫苗監管負責人Vinay Prasad周二在《新英格蘭醫學雜誌》發表的評論,今年秋季的疫苗加強針供應將主要聚焦於65歲以上長者以及患有高風險疾病的人群,對健康的65歲以下人群則將推遲接種,待相關藥廠完成新的隨機對照試驗後再行決定。
據外媒報道,FDA計劃僅根據免疫反應數據批准長者接種新一輪加強針,同時允許六個月以上、具有一種或多種重症風險因素的人群接種。不過,對於六個月至64歲之間的健康族群,FDA將要求疫苗廠商進行新一輪隨機安慰劑對照試驗,以驗證年度接種是否仍具實質效益。Makary與Prasad指出,目前尚無數據能說明,過去已感染數次、並已接種多劑疫苗的健康成年人是否會從第七劑疫苗中獲益。
此舉可能將影響2025至2026年度疫苗配方的設計與推廣節奏。根據周二提交的文件,FDA顧問小組將於本周四召開會議,討論下一年度新冠疫苗是否應針對目前浮現的LP.8.1亞變種。此變種已被視為新一輪疫苗的重要目標,顧問將根據現有病毒監測與免疫資料提供建議。
疫苗股普漲
儘管藥廠擔心,每年依病毒株調整疫苗配方並要求新試驗,將導致產品上市延誤,甚至錯過病毒高峰期,不過FDA強調,有必要確保疫苗政策對年輕健康族群的實際保護效果是基於科學證據。
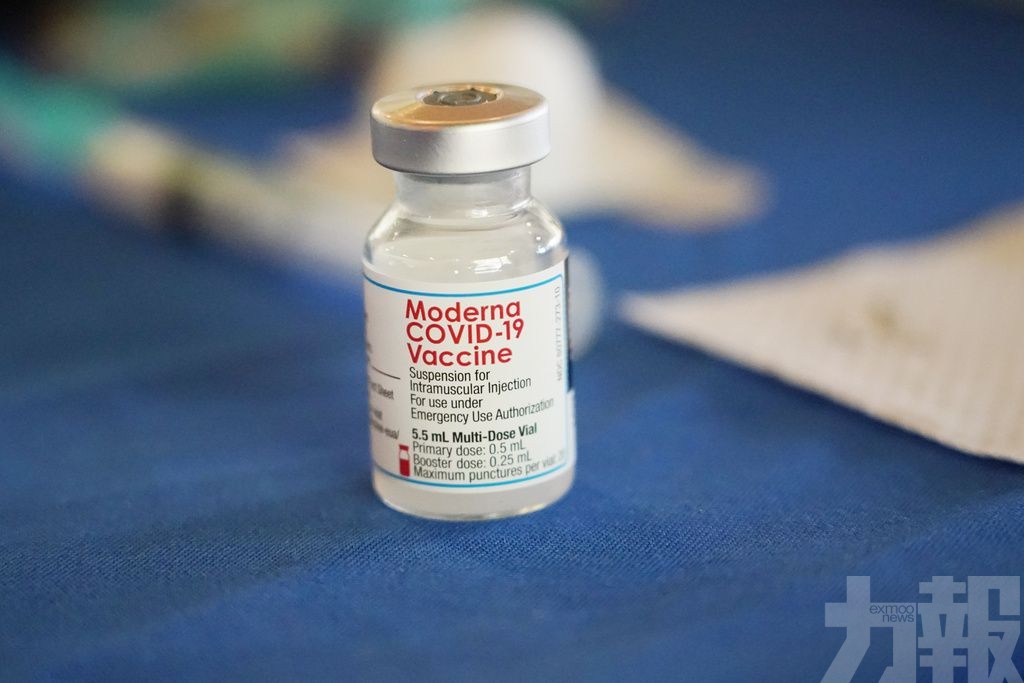
目前,美國已有三款新冠疫苗獲批使用,包括Moderna與Pfizer-BioNTech的mRNA疫苗,以及Novavax的重組蛋白疫苗。
受政策調整與疫情升溫消息帶動,疫苗股周二普遍上揚。Moderna股價一度急升逾10%,收市報27.99美元,升6.06%;Novavax漲超2%,收市微跌0.78%,報7.68美元;輝瑞收升2.26%,報23.52美元。
另一方面,根據世界衛生組織(WHO)近日發布的報告,西非、中美洲、加勒比地區,以及歐洲東部、西南歐與西亞部分國家近期新冠疫情出現回升趨勢,病毒新變異株的出現或將持續推動疫苗需求上升,也為各國公共衛生政策與疫苗儲備敲響警鐘。
此輪FDA針對疫苗審批標準的重新調整,標誌著美國公共衛生政策正從疫情急性階段,邁向以風險分層為核心的常態化管理模式,未來疫苗的推廣、定價與研發策略或將隨之改變。市場亦將密切關注FDA本週四會議的最終建議結果。 (編輯部)